강원대학교(총장 정재연) 농업생명과학대학 스마트팜융합바이오시스템공학과 임기택 교수 연구팀이 가천대학교 화공생명공학과 김종성 교수팀, 한국교통대학교 화공생물공학과 이용규 교수팀과의 공동 연구를 통해 ‘만성 상처와 항생제 내성균 감염을 흉터 없이 치료하는 피부 모사형 스마트 DNA 패치’ 개발에 성공했다.

이번 연구 성과는 바이오소재 분야 세계 최고 권위 학술지인「Bioactive Materials」(Impact Factor 20.3, JCR 상위 2%, JCI 상위 1%) 2026년 3월호에 게재되며 학계의 주목을 받고 있다.
임기택 교수 연구팀이 개발한 스마트 DNA 패치는 만성 상처 치료의 가장 큰 난제로 꼽히는 항생제 내성균 감염과 흉터 형성 문제를 동시에 해결할 수 있는 차세대 창상 치료 플랫폼으로, 특히 치료가 까다로운 메티실린 내성 황색포도상구균(MRSA) 감염 상처에서 탁월한 치유 효과를 입증했다.
당뇨병성 만성 상처는 약제 내성균 감염과 과도한 산화 스트레스가 복합적으로 작용해 치유가 지연되고 심각한 흉터를 남기는 경우가 많았다.
특히, 기존 항생제 연고는 상처 부위의 낮은 pH 환경과 내성균 존재로 인해 항균 활성이 급격히 저하돼, 감염 억제와 조직 재생을 동시에 달성하는 데 구조적 한계를 보여 왔다.
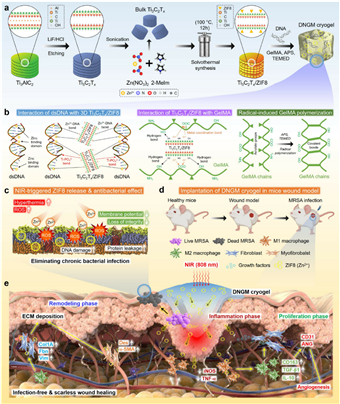
연구팀은 이러한 기존 항생제 기반 치료의 한계를 극복하기 위해, 연어 유래 DNA, 젤라틴 메타크릴레이트(GelMA)를 기반으로 2차원 나노물질인 맥신(MXene)과 금속-유기 골격체 ZIF-8(MOF)를 결합한 광감각형 ‘스마트 DNA 패치’를 개발했다.
연구팀은 해당 패치를 상처 부위에 부착한 뒤 근적외선(NIR)을 쬐는 실험을 실시했으며, ▲맥신의 광열 효과를 통한 박테리아 사멸 효과 ▲ZIF-8에서 방출된 아연 이온(Zn²⁺)이 피부 재생 유전자를 활성화하는 ‘광바이오모듈레이션(Photobiomodulation)’을 동시에 확인했다.
연구 결과, 패치에서 방출된 아연 이온은 세포 내 아연 집게 단백질(Znf) 발현을 유도해 케라틴 세포의 분화와 이동을 촉진했으며, 실제 인간 피부 표피와 유사한 라멜라 기공 구조는 면역세포인 대식세포를 염증형(M1)에서 재생형(M2)으로 전환시켜 과도한 염증 반응을 억제하고 조직 재생을 가속하는 것으로 나타났다.
동물실험 결과, 스마트 DNA 패치 치료군은 대조군 대비 94.85%의 높은 상처 폐쇄율을 기록했으며, 단순한 상처 회복을 넘어 ▲정상 피부와 유사한 두꺼운 표피 형성 ▲신생 혈관 증식 ▲모낭(Hair follicle) 재생까지 확인됐다.
또한 재생된 피부의 인장 강도는 정상 피부 수준에 근접했으며, 체내 삽입 후 21일 이내 완전 생분해되고 주요 장기에 독성을 남기지 않아 높은 생체 안전성도 입증됐다.
임기택 교수 연구팀은 첨단 전사체(Transcriptome) 분석을 통해 ‘흉터 없는 재생’의 분자 수준 치유 메커니즘을 규명했다.
임기택 교수는 “이번 연구는 인공 피부 기술과 나노 기술을 융합해 만성 상처 치료의 고질적인 문제인 감염과 흉터를 동시에 해결한 혁신적 성과”라며 “향후 고부가가치 창상 피복제는 물론, 재생의학 및 스마트 바이오 의료소재 분야 전반으로의 확장 가능성이 크다”고 밝혔다.
한편, 이번 연구는 한국연구재단의 ‘중견연구지원사업’· 지역지능화혁신인재양성사업과 산림과학연구소의 ‘대학중점연구소지원사업’의 지원을 받아 수행됐다.




전체댓글 0